Introdução
A congelação do sêmen suíno permite a difusão e conservação de doses inseminantes de alto valor genético e apresenta-se como uma alternativa para as situções nas quais o movimento de animais e sêmen é restrito, além de controlar a propagação de doenças sexualmente transmissíveis, portanto, o alcanço do sucesso na criopreservação pode representar um importante avanço no sistema de produção de suínos (1, 2). Entretanto, a qualidade do sêmen criopreservado de suíno ainda é muito baixa, com baixos percentuais de integridade das membranas espermáticas, as quais são essenciais em vários processos biológicos, como por exemplo, na fertilização do oócito e exocitose das enzimas do acrossoma. Inexistem trabalhos na literatura sobre qual a concentração espermática ideal na palheta de 0,5mL para melhor conservar os espermatozoides suínos, mantendo uma melhor integridade das membranas espermáticas. Salienta-se que quanto maior a concentração de espermatozoides na palheta menor seria o número de palhetas descongeladas para obter a dose inseminante (1,5 x 106 – 3 x 106 espermatozoides). Com isso, este experimento teve por objetivo avaliar, através da citometria de fluxo, a integridade das membranas plasmática e acrossomal do espermatozoide suíno pós descongelação, congelado em 5 diferentes concentrações: 100x106, 200x106, 300x106, 600x106 e 800x106 espermatozoides/mL, em palhetas de 0,5 mL.
Material e Método
Foram utilizados cinco cachaços híbridos comerciais, Agroceres PIC®. A fração rica de cinco ejaculados suínos foram coletadas através do método da mão enluvada com prévia higienização do prepúcio. Somente ejaculados com motilidade total acima de 75 % e alterações morfológicas abaixo de 20 % foram submetidos à congelação. A concentração espermática foi determinada, em milhões de espermatozoides por mililitro (mL), com auxílio da Câmara de Neubauer, sob microscopia óptica comum (Nikon – Eclipse E200®), em aumento de 400x. Realizadas as análises iniciais do sêmen (in natura) este foi diluído em meio Botusui® (Botupharma®, Botucatu-SP, Brasil) a fim de se obter cinco diferentes concentrações: 100 x 106, 200 x 106, 300 x 106 , 600 x 106 e 800 x 106 espermatozoides/ mL. O sêmen diluído foi envasado em palhetas de 0,5 mL (IMV Internacional, St. Paul, Minesota, USA) e submetidos à congelação em sistema automático (TK 3000 compacta®, TK Tecnologia em Congelação Ltda, Uberaba, Minas Gerais, Brasil), e as palhetas congeladas foram raqueadas e armazenadas em botijões criogênicos. Duas palhetas por partida foram descongeladas, a 37°C por 30 segundos em banho-maria, e avaliadas por citometria de fluxo (FACSAria® BD Bioscience®, USA) com auxílio das sondas fluorescente Hoechst 33342 (2,3 μg/mL), iodeto de propídeo (100 μg/mL), FITC-PSA (13,3 μg/mL) e JC-1 (4,1 μM) quando a integridade das membranas plasmática e acrossomal e potencial de membrana mitocondrial (3). Este experimento foi delineado em blocos generalizados, sendo cada cachaço considerado um bloco. A unidade experimental foi considerada 1/5 do ejaculado. Os dados foram submetidos à análise de variância (PROC MIXED), empregando-se o programa SAS (2002). Os tratamentos foram avaliados pelo teste de médias PDDIF do PROC MIXED do programa SAS (2002). Foi considerado o nível de 5 % de significância.
Resultados e Discussão
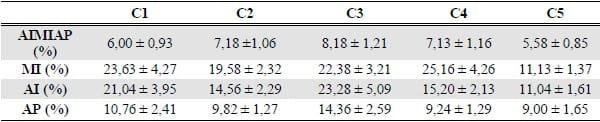
A qualidade espermática, em relação a integridade das membranas plasmática e acrossomal e potencial de membrana mitocondrial não é alterada pelo aumento da concentração espermática, até 800 x 106 espermatozoides/mL. Entretanto, quando utilizou-se uma concentração de 300 x 106 espermatozoides/mL o percentual das células espermáticas com as membranas plasmática e acrossomal íntegras e alto potencial de membrana mitocondrial (AIMIAP) foi numericamente maior que as demais concentrações estudadas (tabela 1). Em estudo anterior, de nosso grupo de pesquisa (4), foi possível demonstrar que os espermatozoides de suíno, criopreservado nas mesmas condições que o presente experimento, apresentam melhores valores de motilidade total e progressiva (%) quando congelados em concentrações até 300 x 106 espermatozoides/mL. Tal fato pode ter ocorrido em decorrência da proporção diluidor : célula espermática, a qual é abruptamente diminuída com o aumento da concentração de espermatozoides/ mL. Por outro lado, no presente trabalho, não foi possível demonstrar o efeito deletério, sobre a integridade das membranas espermáticas, do aumento da concentração espermática na palheta de 0,5 mL.
Tabela 1 – Média ± erro padrão da média das variáveis de integridade das membranas espermáticas, avaliadas por citometria de fluxo, de espermatozoides suínos submetidos à criopreservação em cinco diferentes concentrações em palhetas de 0,5 mL. AIMIAP (membrana plasmática e acrossomal integras e alto potencial de membrana mitocondrial), MI (membrana plasmática íntegra), AI (acrossoma íntegro) e AP (alto potencial de membrana mitocondrial).
Conclusão
De acordo com os resultados apresentados, podemos concluir que é possível realizar a congelação do sêmen suíno em palhetas de 0,5mL, com um concentração espermática de até 800 x 106 espermatozoides/mL sem que as membranas plasmática e acrossomal e o potencial de membrana mitocondrial sejam prejudicados.
Agradecimentos
À FAPESP Processo 2011/23484-8 e a Botupharma®.
Referências Bibliográficas
1.BAILEY, J. L; LESSARD, C.; JACQUESS, J.; DOBRINSKI, I.; ZENG, W. Cryopreservation of boar semen and its future importance to the industry. Therio, v. 70, p. 1251-1259, 2008.
2.VELLOSO, N. M. Congelação e efeito do meio sobre as características físico-químicas do sêmen suíno no inverno e verão. 2011. 97 f. Tese (Doutora em Reprodução Animal) – Faculdade de Medicina Veterinária e Zootécnica, Universidade Estadual Paulista, Botucatu, 2011.
3. TORRES, M.A; BIGUEN, R; DÍAZ, R; SEPULVEDA, N; DE ANDRADE, A.F.C. Validación de la técnica de coloración cuadruple por citometria de flujo: evaluación simultanea de la integridad de las membranas plasmática y acrosomal y potencial de membrana mitocondrial de los espermatozoides porcinos. Primer Congress de la Sociedad Latino Americana de Reproducción Animal, v.1; p.267-270; 2015. Buenos Aires - AR.
4. RAVAGNANI, G.M; TORRES, M.A; OLIVEIRA, M.L.; LEAL, D.F.; DE CAMPOS, G.A., MURO, B.B.D., MORETTI, A.S.; PAPA, F.O.; MARTINS, S.M.M.K.; DE ANDRADE, A.F.C. Efeitos da congelação do sêmen suíno armazenado em diferentes concentrações na palheta de 0,5mL. XXVIII Reunião da Sociedade Brasileira de Tecnologia de Embriões, 2014, Natal-RN.
***O TRABALHO FOI ORIGINALMENTE APRESENTADO DURANTE O XVII CONGRESSO ABRAVES 2015- SUINOCULTURA EM TRANSFORMAÇÂO, ENTRE OS DIAS 20 e 23 DE OUTUBRO, EM CAMPINAS, SP.