INTRODUÇÃO
Fungos, também denominados mofos ou bolores, são microrganismos eucarióticos como as leveduras, são multicelulares e filamentosos. É de conhecimento secular que a atividade de fungos ocasiona alterações no sabor e na qualidade dos alimentos. Algumas destas alterações são desejáveis, como na fabricação de queijos. Todavia, em muitos casos, os fungos podem causar transformações indesejáveis nos alimentos, produzindo sabores e odores desagradáveis, causados por diferentes graus de deterioração (Diniz, 2002).
Alguns gêneros de fungos podem produzir micotoxinas, entre as quais, destacam-se a aflatoxina, ocratoxina, zearalenona, patulina, fumonisina e desoxinivalenol (Hussein & Brassel, 2001; Rodríguez-Amaya & Sabino, 2002; Murphy et al., 2006). As micotoxinas são metabólitos secundários, de baixo peso molecular, produzidos por fungos; apresentam efeito tóxico para o homem e outros vertebrados, além de alguns invertebrados, plantas e microrganismos (Bennett & Klich, 2003).
Diferentes espécies de fungos podem produzir um mesmo tipo de micotoxina, como também, uma única espécie de fungo pode produzir mais de um tipo de toxina. Os efeitos tóxicos das micotoxinas podem ser potencializados pelo sinergismo que pode haver entre elas ou com doenças, principalmente imunossupressoras (Hussein & Brassel, 2001).
Para os fungos se desenvolverem e produzirem micotoxinas são necessárias condições favoráveis de umidade, temperatura, pH, composição química do alimento e potencial redox (Pereira et al., 2002). A presença do fungo no alimento não implica, obrigatoriamente, em produção de micotoxina, assim como, a toxina pode estar presente no alimento mesmo na ausência do fungo (Diniz, 2002). Isto porque a maioria das micotoxinas são termoestáveis, resistindo a determinados tratamentos térmicos ou processos de desidratação que são suficientes para destruir o micélio vegetativo dos fungos que as produziram (Molin & Valentini, 1999).
As micotoxinas podem entrar na cadeia alimentar humana direta ou indiretamente. Diretamente, através do consumo dos cereais, oleaginosas e derivados. Os animais que se alimentam com rações previamente contaminadas podem excretar micotoxinas no leite, carne e ovos, e consequentemente, constituir-se em fonte de contaminação indireta para os humanos (Molin & Valentini, 1999).
A ingestão de alimentos que contenham micotoxinas pode causar graves efeitos sobre a saúde animal e humana (Pitt, 2000; Shephard, 2008). Tais efeitos são conhecidos como micotoxicoses, cuja gravidade depende da toxicidade da micotoxina, grau de exposição, idade e estado nutricional do indivíduo, e dos possíveis efeitos sinérgicos de outros agentes químicos aos quais está exposto (Peraica et al., 2000, Bhatnagar et al., 2002).
Sua entrada no organismo comumente se dá pela via digestiva e sua absorção geralmente causa reações sob a forma de hemorragias, ou mesmo, necroses. Muitas destas toxinas têm afinidade por determinado órgão ou tecido, sendo o fígado, os rins e o sistema nervoso freqüentemente os mais atingidos (Santurio, 2000).
O efeito de uma micotoxina depende da dose e da freqüência com que é ingerida e pode ser agudo (letal ou não) ou subagudo. O efeito agudo é de manifestação e percepção rápidas, podendo levar à morte, porque causa alterações irreversíveis, e é resultante da ingestão de doses geralmente elevadas. O efeito subagudo é o resultado de doses menores que provocam distúrbios e alterações nos órgãos dos humanos e dos animais (Bennett & Klich, 2003; Murphy et al., 2006; Shephard, 2008).
As condições climáticas de um país determinam, em grande parte, as classes de fungos que irão crescer e os tipos de micotoxinas que podem produzir. No Brasil, existem condições propícias para o crescimento de todo tipo de fungos produtores de micotoxinas.
O Conselho Nacional de Desenvolvimento Científico e Tecnológico – CNPq possui vários grupos de pesquisa cadastrados no Brasil que dedicam seus estudos na avaliação de alimentos in natura, industrializados e em desenvolvimento quanto à contaminação fúngica e micotoxicológica e no desenvolvimento de novas metodologias de detecção de micotoxinas.
A presente revisão tem como objetivo relatar algumas das pesquisas que estão sendo feitas no Brasil com micotoxinas em alimentos, ressaltando assim a importância destes estudos e de conhecermos a realidade dos produtos brasileiros com relação a elas.
Principais micotoxinas encontradas nos alimentos.
As micotoxinas são produzidas principalmente por cinco gêneros de fungos: Aspergillus, Penicillium, Fusarium, Claviceps e Alternaria. As principais micotoxinas encontradas em alimentos são: aflatoxinas (B1, B2, G1, G2 e M1), ácido fusárico, fumonisinas (B1 e B2), fumonisinas, ocratoxinas (A, B e C), patulina, citrinina, zearalenona e tricotecenos.
Aflatoxinas são encontradas em frutas secas e cereais em condições de umidade e temperatura elevadas e constituem um risco a saúde humana, devido aos seus efeitos tóxicos imediatos, imunossupressores, mutagênicos, teratogênicos e carcinogênicos. As espécies mais importantes de Aspergillus produtoras de aflatoxinas são A. flavus, que só produz AFB, e A. parasiticus, que produz AFB e AFG (Peraica et al., 2000). A aflatoxina M1 é um metabólito da aflatoxina B1, encontrada no leite e urina de animais alimentados com rações contaminadas (Richard, 2007).
A aflatoxina tem recebido grande atenção em comparação com as demais micotoxinas, devido aos efeitos carcinogênicos que podem provocar em animais e o efeito agudo tóxico em seres humanos. As aflatoxinas representam o grupo de micotoxinas com mais resultados positivos em alimentos já relatados (Pereira et al., 2002).
Fumonisina é produzida pelas cepas de Fusarium moliniforme, encontrada principalmente em milho. A fumonisina pode ser fatal para alguns animais, como os eqüinos, nos quais causa a leucoencefalomalacia, que se caracteriza pela formação de cavitações na substância branca do cérebro, acompanhada de amolecimento da mesma, resultando em morte. O efeito das fumonisinas em humanos não estão bem esclarecidos, no entanto, evidências sugerem a ocorrência de câncer de esôfago (Pitt, 2000).
Patulina é um metabólito secundário produzido por diferentes gêneros e espécies de fungos, entre eles o mais importante é o Penicillium expansum, um contaminante comum de maçãs e outras frutas. O fungo desenvolve-se em partes da fruta danificadas mecanicamente ou por pragas, onde se observa o apodrecimento; todavia, a patulina pode ser detectada em frutas visivelmente sadias. Experimentos em animais de laboratório demonstraram que esta micotoxina produz diversos efeitos nocivos, incluindo mutagenicidade, teratogenicidade, carcinogenicidade, imunossupressão e intoxicações agudas caracterizadas por edema pulmonar, hemorragias, danos nos capilares hepáticos, do baço e rins, bem como edema cerebral (Pádua & Machinski Junior, 2005).
Ocratoxinas são produzidas por cepas de Aspergillus e Penicillium presentes em cereais, café e pão. A ocratoxina A é a mais freqüente e a mais tóxica. Apresenta efeitos nefrotóxicos, imunossupressores, carcinogênicos e teratogênicos (Peraica et al., 2000; Murphy et al., 2006).
Os tricotecenos são um grupo de mais de cem micotoxinas e possuem esse nome devido a sua estrutura química, composta de um anel com esqueleto tetracíclico 12,13-epoxitricotecenos. Essas toxinas são classificadas em tipo A, na qual se encontram as toxinas T-2, HT-2, 15-monoacetoxiscirpenol (15-MAS) e diacetoxiscirpenol (DAS), e em tipo B, na qual está o desoxinilvalenol (DON ou vomitoxina) (Santin et al., 2000). Deoxinivalenol é produzida principalmente por Fusarium graminearum e, em algumas regiões, por F. culmorum. DON pode coexistir com zearalenona, também produzida por estes microrganismos (Richard, 2007).
O ácido fusárico é, provavelmente, uma das micotoxinas mais distribuídas na natureza uma vez que ela é produzida pela maioria das espécies do gênero Fusarium. O ácido fusárico possui a capacidade de aumentar a toxicidade de outras micotoxinas, e como não poderia ser diferente, essa micotoxina dificilmente aparece isolada em grãos contaminados por Fusarium, o que faz com que aumente sua importância nas micotoxicoses (Santin et al., 2000).
Zearalenona é produzida principalmente por Fusarium graminearum, sobretudo em trigo e milho, mas também em sorgo, cevada e rações animais. A zearalenona e seus derivados têm efeitos estrogênicos em várias espécies animais (infertilidade, edema vulvar, prolápso vaginal e hipertrofia mamária em fêmeas e feminização de machos, atrofia testicular e aumento de tamanho das glândulas mamárias) (Peraica et al., 2000).
Legislação para micotoxinas no Brasil
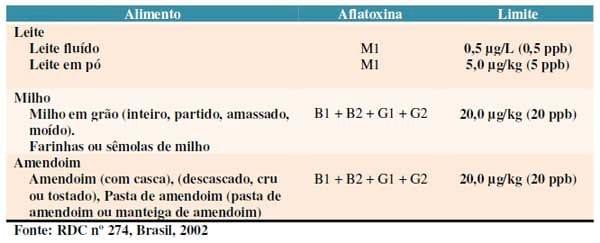
No Brasil, as aflatoxinas são as únicas micotoxinas cujos limites máximos em alimentos são previstos na legislação. Em 2002, foi publicado no Diário Oficial da União a resolução RDC nº 274 da Agência Nacional de Vigilância Sanitária (ANVISA) que estabelece os limites máximos de aflatoxinas admissíveis no leite fluído, no leite em pó, no amendoim, na pasta de amendoim, no milho em grão, na farinha ou sêmola de milho para consumo humano, bem como os planos de amostragem e métodos de análise correspondentes (Brasil, 2002).
Para os demais produtos alimentícios destinados ao consumo humano, ainda prevalece a legislação de 1974, do Ministério da Saúde, Comissão Nacional de Normas e Padrões para Alimentos Resolução no 34/76, publicada no Diário Oficial da União, em 19 de janeiro de 1977, no qual o limite de aflatoxinas B1 + G1 é de 30 μg/kg (30 ppb) (Brasil, 1977).
Os limites indicados no Quadro 01 são adotados pelos demais países do MERCOSUL (Argentina, Paraguai e Uruguai). Outros países têm seus limites estabelecidos de acordo com o Codex Alimentarius ou legislações específicas, como a União Européia e o Food and Drug Administration (FDA) nos Estados Unidos.
Quadro 1: Limites máximos admissíveis de concentração de aflatoxinas no Brasil.
Atualmente existem kits de ELISA (Enzyme-linked immunosorbent assay) para análise das principais micotoxinas, porém, as reações falso-positivas dificultam ainda, a sua utilização como alternativa aos métodos reconhecidos pela AOAC (Association of official analytical chemists), sendo necessária a confirmação por métodos químicos como a Cromatografia Líquida de Alta Eficiência (CLAE). Os imunoensaios desempenham um papel importante na análise de micotoxinas, pois disponibilizam uma gama de métodos que podem ser utilizados tanto nos laboratórios como ensaios quantitativos, como no campo, para triagem (Ono et al., 2004).
Micotoxinas em alimentos produzidos no Brasil
Grãos, cereais e derivados
Rodríguez-Amaya e Sabino (2002) realizaram uma intensa revisão bibliográfica sobre a presença de micotoxinas em alimentos coletados no período de 1991 a 2000 no Brasil e alertaram sobre os altos índices de aflatoxinas em amendoim e produtos de amendoim, e pela alta incidência e níveis elevados de fumonisinas em milho e produtos de milho. No entanto, as demais micotoxinas, como a zearalenona, ocratoxina A e tricotecenos, apresentaram baixos índices de contaminação.
A pesquisa de Caldas et al. (2002) reforça esta afirmação; os autores avaliaram 366 amostras de amendoim, castanhas, milho e farinhas obtidas no comércio do Distrito Federal quanto à presença de aflatoxinas e ocratoxina A. Foram detectadas aflatoxinas em 19,6% das amostras, sendo que o amendoim e derivados apresentaram maior incidência de contaminação (34,7%), contendo até 1.706 ppb de aflatoxinas totais. Ocratoxina A não foi detectada (<25 ppb) em nenhuma amostra analisada.
Uma pesquisa mais recente avaliou a presença de micotoxinas em amostras de amendoim coletadas em diferentes etapas da produção; 32% das amostras apresentaram contaminação por aflatoxina B1 e B2, com concentrações variando entre 3,79 a 125,07 ppb e 0,07 a 2,3 ppb, respectivamente (Gonçalez et al., 2008).
Em 2002, a Vigilância Sanitária no Paraná coletou 38 amostras de doces de amendoim para determinação de aflatoxinas B1, B2, G1 e G2. 73,68% das amostras de doces de amendoim estavam contaminadas com aflatoxinas numa faixa de 25,95 a 350,02 mg/kg para soma de B1 e G1; e 15,79% ultrapassaram o limite de 20 mg/kg para a soma de B1, B2, G1 e G2 estabelecido pela Resolução nº 274 / ANVISA (Einzendeher et al., 2005).
A ocorrência de aflatoxinas é maior no amendoim devido à afinidade do Aspergillus flavus por este alimento e, principalmente, quando as condições de umidade e temperatura são favoráveis ao seu crescimento (Diniz, 2002).
O Laboratório de Análises Micotoxicológicas (LAMIC) no Rio Grande do Sul, avaliou amostras de nozes (castanhas, nozes e amêndoas) e de frutas secas (uvas passas, damascos, ameixas secas e pêras secas) comercializadas no Brasil no ano de 2002. Das amostras analisadas, 10,8% apresentaram contaminação por aflatoxinas. As nozes apresentaram 21,7% de positividade, seguida das frutas secas com 7,1% (Mallmann et al., 2003b). No entanto, Freire et al. (1999) não detectaram aflatoxinas nas amostras de castanha de caju avaliadas no Ceará, apesar de identificarem 37 espécies de fungos nestas amostras.
A presença de aflatoxinas foi avaliada em 62 amostras de frutas secas comercializadas em São Paulo e importadas da Argentina, Chile, Irã e Turkia. Foram detectadas aflatoxinas em três de 19 (16%) das amostras de uvas passas brancas, com limite não superior a 2 ppb. Onze de 19 amostras (58%) de figo seco apresentaram aflatoxinas e, com exceção de uma amostra que apresentou 1500 ppb de aflatoxina B1, as demais não ultrapassaram 2 ppb. Nenhuma das 24 amostras de uvas passas pretas apresentaram aflatoxinas (Iamanaka et al., 2007).
No Brasil, varias pesquisas se concentram na avaliação da presença de micotoxinas em grãos e cereais. Mallmann et al. (2001b) avaliaram os níveis de fumonisina B1 em 407 amostras vários cereais (milho, arroz, trigo, cevada, aveia e farelo de soja) na região sul do Brasil. Das amostras analisadas, 32% apresentaram positividade. As maiores concentrações foram encontradas no arroz, 14,21 ppm; trigo, 24,35 ppm; e cevada, 2,43 ppm.
Foram analisadas 68 amostras de arroz em São Paulo e não foi encontrada ocratoxina A em nenhuma delas. Aflatoxina B1 foi detectada em 2,9% das amostras de arroz polido tipo 1, com teores variando de 9 e 6 ppb e uma das amostras apresentou traços de aflatoxina B2 (Simionato et al., 2003). Na região sul do Brasil 56 amostras de arroz (integral, polido e parboilizado) destinado ao consumo humano foram avaliadas quanto à contaminação por ocratoxina A, zearalenona de desoxinivalenol. Dentre as amostras analisadas, duas apresentaram contaminação por ocratoxina (102 e 128 ppb), três por zearalenona (550, 1117 e 1955 ppb), e uma por desoxinivalenol (300 ppb). Considerando o hábito alimentar brasileiro de consumir arroz quase diariamente torna-se necessário o monitoramento deste produto e o estabelecimento de uma legislação específica (Nunes et al. 2003).
O arroz parboilizado pode apresentar maiores índices de contaminação, uma vez que as micotoxinas presentes na casca podem migrar para o interior do grão durante o processo de parboilização (Dors et al., 2009).
Calori-Domingues et al. (2007) avaliaram 50 amostras de trigo provenientes dos Estados de São Paulo, Paraná e Rio Grande do Sul e 50 amostras de trigo importado (Argentina e Paraguai) comercializado no Brasil quanto à presença de desoxinivalenol (DON). Do total de amostras avaliadas, 94% do trigo nacional e 88% do trigo importado apresentaram-se contaminados com DON em níveis médios de 332 μg/kg (nacional) e 90 μg/kg (importado). Apenas 4% das amostras de trigo nacional apresentaram níveis de DON maiores de 1.250 ppb, limite máximo aceito pela Comunidade Européia.
No sul do Brasil, 24,91% das 297 amostras de trigo utilizado na alimentação humana apresentaram contaminação por Desoxinivalenol, com nível médio de 603,2 ppb e máximo de 8504 ppb (Malmann et al., 2003a). Outro estudo feito em São Paulo apresentou contaminação por DON em 45% das 42 amostras de trigo analisadas em níveis que variaram de 82 a 1500 ppb (Lamardo et al., 2006).
Pinho e Furlong (2000) avaliaram a presença de micotoxinas em massa de pizza pré-fabricada e, embora não tenha sido detectada nenhuma micotoxina, foi isolada uma cepa do gênero Penicillium em várias amostras, que produziu ocratoxina A em refrigeração.
A prevalência de desoxinivalenol em 1103 amostras de alimentos consumidos no Brasil analisados entre 1999 e 2001 foi de 12,24%, sendo que o cereal mais contaminado foi a cevada (28,35%), apresentando nível máximo de 5,2 ppm, seguida pelo malte (27,19%) e milho (5,7%) (Mallmann et al. 2001a). Foram constatadas cinco das 90 amostras (5,56%) de milho tipo pipoca avaliadas em Campinas contaminadas por desoxinivalenol, sendo que os níveis variaram de 30 a 40 ppb. Não foram detectadas Diacetoxiscirpenol e Toxina T2 nas amostras avaliadas (Oliveira et al., 2001).
A ocorrência de micotoxinas em milho e produtos a base de milho tem sido reportada por vários autores, principalmente em se tratando de aflatoxina e fumonisina (Amaral et al., 2006; Kawashima & Valente soares, 2006; Sekiyama et al., 2005; Camargos et al., 2000, Fick et al., 2003, Machinski et al., 2001, Caldas & Silva, 2007).
Amostras de diversos produtos de milho, entre eles, fubá, farinha de milho, pipoca, canjica, corn flakes, salgadinhos de milho e polenta pronta comercializados no norte do Paraná apresentaram baixa incidência de aflatoxinas, com contaminação média variando de 0,62 a 0,78 ppb (Amaral et al., 2006).
A presença de fumonisina B1, aflatoxinas B1, B2, G1 e G2, ocratoxina A e zearalenona foi avaliada em 74 amostras de produtos a base de milho adquiridas no comércio da cidade de Recife, PE, durante o período de 1999 a 2001. Fumonisina B1 foi encontrada em 94,6% das amostras em concentrações variando de 20 a 8.600 ppb; 6,76% das amostras continham aflatoxina B1 e o teor máximo encontrado foi 20 ppb. As aflatoxinas G1 e G2, ocratoxina A e zearalenona não foram detectadas em nenhuma das amostras. Todas as amostras contaminadas com aflatoxinas também apresentaram fumonisina B1 (Kawashima & Valente Soares, 2006).
Caldas & Silva (2007) avaliaram 208 amostras de 10 diferentes produtos a base de milho comercializados no Distrito Federal e econtraram 80,7 e 71,6% das amostras contaminadas com FB1 e FB2, respectivamente.
A ocorrência de aflatoxinas B11 (AFB1), B2 (AFB2), G1 (AFG1) e G2 (AFG2), ocratoxina A (OA) e zearalenona (ZEA) foi avaliada em 121 amostras de alimentos a base de milho coletadas no comércio da Cidade de Maringá, Paraná. Três amostras (2,5%) foram positivas para AFB1 (8 a 59 ppb), duas (1,7%) para AFB2 (2,4 ppb), uma (0,8%) para OA (64 ppb) e uma (0,8%) para ZEA (448 ppb). A maior freqüência positiva e maior concentração encontrada de AFB1 foi para milho pipoca (8,3%, 59 ppb) (Sekiyama et al., 2005).
Dezenove cultivares de milho das Estações Experimentais do Instituto Agronômico de São Paulo foram avaliados quanto à presença de fumonisinas. Todos os cultivares analisados estavam contaminados com fumonisinas em níveis que variaram de 1,63 ppm a 25,69 ppm e uma média de 5,61 ppm Fumonisina B1 e de 0,38 ppm a 8,60 ppm e uma média de 1,86 ppm para Fumonisina B2 (Camargos et al., 2000).
Os tricotecenos deoxinivalenol (DON), nivalenol (NIV), diacetoxiscirpenol (DAS) e as toxinas T2 e HT2 foram avaliadas em 78 amostras de produtos a base de milho comercializados na cidade de São Paulo. Somente duas amostras apresentaram contaminação, uma amostra de milho moído com 555 ppb de T2 e 767 ppb de HT2 e outra amostra de farinha de milho apresentou traços de DON e NIV. DAS não foi detectado em nenhuma amostra (Milanez et al., 2006).
Machinski et al. (2001) avaliaram 110 amostras de milho recém-colhido no estado de São Paulo e encontraram 54,5% das amostras contaminadas com aflatoxina B1, com níveis variando de 6 a 1600 ppb. Ocratoxina A foi encontrada em 2 amostras (206 e 128 ppb) e zearalenona em uma amostra (4640 ppb).
As 333 amostras de soja avaliadas no sul do Brasil entre 2000 e 2003 apresentaram 15,01% de positividade para aflatoxinas com média de 3,99 ppb e máxima de 33 ppb (Mürmann et al., 2003).
A amostragem é um fator preponderante nas determinações de micotoxinas, devido à distribuição heterogênea das toxinas, nos grãos principalmente. Planos de amostragem para análise de micotoxinas em grãos devem ser feitos por meio de fórmulas de acordo com o tamanho do lote (Fonseca, 2002).
Produtos de origem animal
Considerando que o milho, a soja e outros cereais são a base da dieta animal, a contaminação da ração por micotoxinas provoca alterações patológicas e implicações no desempenho zootécnico, causando grande impacto econômico na produção animal (Santúrio, 2000; Santin et al., 2000, Rosmaninho et al., 2001).
A aflatoxina B1, quando ingerida, é biotransformada no fígado em aflatoxina M1, podendo ambas ser encontradas no fígado de aves (Silveira et al., 1996). Quarenta amostras de fígado de aves produzidas e comercializadas em Pernambuco apresentaram contaminação por aflatoxinas (B1, B2, G1 e G2) em todas as amostras em concentrações inferiores a 5 ppb, que é o limite de quantificação do método. Zearalenona e ocratoxina A não foram detectadas (Vilar et al., 2002).
Stamford et al. (2005) avaliaram 54 amostras de produtos avícolas in natura e processados obtidos em diferentes Estados do Brasil quanto à presença de aflatoxina e ocratoxina A; 12% das amostras analisadas foram positivas, sendo 10,8% para aflatoxina total (médias variando de 1,4 ppb a 5,2 ppb) e 1,2% para ocratoxina A (médias de 4,0 ppm a 5,4 ppm). Do total de amostras positivas, os produtos in natura (fígados e coxas) apresentaram os maiores índices de contaminação (57,2%).
Resíduos de aflatoxina também podem ser encontrados em ovos obtidos de aves alimentadas com rações contendo aflatoxina (Oliveira et al., 2000). A detecção de aflatoxina em ovos é dificultada porque as amostras possuem conteúdo elevado de triglicerídios, colesterol, caroteno e proteínas. (Scussel, 2003).
A ocorrência de aflatoxina M1 em leite pasteurizado, esterilizado e em pó consumido na cidade de Belo Horizonte – Minas Gerais foi avaliada no período de agosto de 1998 a abril de 1999. Aflatoxina M1 foi encontrada em 82% de todas as amostras analisadas, mas em níveis inferiores a 0,5 ppb - limite máximo permitido no Brasil (Prado et al., 1999). No Paraná, foram encontradas 24% das 42 amostras de leite cru analisadas contaminadas por aflatoxina M1, sendo 7% destas acima do limite de 0,5 ppb (Sassahara et al., 2005).
Outro estudo feito em Campinas, SP avaliou a presença de aflatoxina M1 em 36 amostras de leite de cabra pasteurizado, UHT e em pó; 69,4% das amostras foram positivas, apresentando níveis variando entre 0,011–0,161 ppb. Estes resultados podem ser considerados impróprios se considerarmos o limite de tolerância recomendado pela União Européia (0,05 ppb) (Oliveira & Ferraz, 2007).
Aflatoxina M1 foi detectada em 39,5% das 43 amostras de leite analisadas no estado de São Paulo, sendo que 64,7% destas amostras apresentavam concentrações acima do limite máximo permitido pela legislação (0,5 ppb) (Gonçalez et al., 2005).
Amostras de queijo Minas (frescal, canastra e padrão) foram avaliadas quanto à presença de aflatoxina M1 e 75% das amostras apresentaram contaminação em níveis de 0,02 a 6,92 ppb (Prado et al., 2000c). Em queijo ralado, tipo parmesão, aflatoxina M1 foi detectada em 93% das 14 marcas analisadas, em faixa de concentração de 0,04 a 0,30 ppb e média de 0,14 ppb (Prado et al., 2001).
Outros alimentos
A contaminação de café verde por ocratoxina foi avaliada por Leoni et al. (2001) em cinco estados brasileiros (Minas Gerais, São Paulo, Paraná, Espírito Santo e Bahia). Os autores encontraram 20,45% das 132 amostras contaminadas, sendo que a concentração média foi de 7,1 ppb de ocratoxina A. Prado et al. (2000a) constataram que as amostras de café solúvel e café torrado e moído comercializados em Belo Horizonte/MG, continham níveis de ocratoxina A entre 0,31 e 1,78 ppb e 0,99 e 5,87 ppb, respectivamente.
Outro estudo feito com 82 amostras de café instantâneo comercializados em São Paulo apresentou 98,8% das amostras contaminadas com ocratoxina A, com níveis variando de 0,17 a 6,20 ppb. A alta freqüência de OTA encontrada nestas amostras ressalta a importância do controle deste produto pela indústria e pelas autoridades (Almeida et al., 2007).
A ocorrência da patulina em uva fina (Vitis vinifera L. cv, "Rubi") com sinais de podridão ácida causada por Penicillium spp. foi avaliada, porém, nas 40 amostras analisadas, não foi detectada contaminação por esta micotoxina (Caldas et al., 2008). Também não foi detectada a presença de patulina em 84 amostras de polpa comercial de tomate, sendo o limite de detecção de 10 ppb (Kawashima et al., 2002).
Treze marcas de suco de maçã comercializadas em Belo Horizonte, MG foram coletadas entre março e setembro de 1999. Patulina foi detectada em apenas uma amostra (10 ppb) (Prado et al., 2000b).
Um estudo feito com 58 amostras de cerveja produzidas em diferentes regiões do Brasil foram avaliadas quanto à presença de fumonisina B1 e ocratoxina A. Fumonisina B1 foi detectada em 25 amostras (43%) das amostras analisadas, em níveis variando de 1 a 40 ppb. Ocratoxina A foi encontrada em níveis que variaram de 1 a 18 ppb, com uma concentração média de 9,6 ± 10,2 ppb. Os autores afirmam que a contaminação da cerveja brasileira por fumonisina B1 e ocratoxina A não representa um problema à saúde do consumidor, porém, no caso de consumo alto e regular, esta pode contribuir substancialmente na ingestão de ocratoxina A, porém, ainda abaixo do máximo considerado tolerável para a toxina (Kawashima et al., 2007).
O levantamento da ocorrência de tricotecenos em cervejas comercializadas no Rio Grande do Sul mostrou que 9,7% das 72 amostras coletadas estavam contaminadas, sendo 5,3% com desoxinivalenol e 4,5% com toxina T-2. Os níveis detectados variaram entre 50-336 ppb e 114-249 ppb respectivamente (Garda et al. 2004).
A presença de Ocratoxina A foi avaliada em 101 amostras de vinho tinto e suco de uva, compradas em supermercados e lojas especializadas na cidade de São Paulo. Os resultados demonstraram uma contaminação por ocratoxina A em 31% das amostras de vinho tinto provenientes do Brasil, com níveis de contaminação variando de 0,10 a 1,33 ppb. Ocratoxina A não foi detectada em nenhuma amostra de suco de uva analisada. Embora os resultados das amostras de vinho analisadas para a presença de ocratoxina A estejam inferiores aos limites máximos estabelecidos pela Comunidade Européia - EC 123/2005 (2,0 ppb), uma exposição pequena e contínua por essa micotoxina pode trazer um sério risco à saúde humana (Shundo et al., 2006).
CONCLUSÃO
O monitoramento de micotoxinas em alimentos é de extrema importância para a saúde pública, visando a adoção de medidas tecnológicas a fim de reduzir a exposição a alimentos considerados de risco para estas toxinas.
As pesquisas realizadas no Brasil nos últimos 10 anos relatam variados índices de contaminação por micotoxinas em diferentes tipos de alimentos, muitos destes ainda sem legislação específica quanto aos limites aceitáveis para tais toxinas.
Historicamente o amendoim tem apresentado elevados índices de contaminação por aflatoxinas, como continuam relatando nas pesquisas feitas no Brasil.
Os grãos e cereais apresentam variados índices de contaminação por diversas micotoxinas, como fumonisina em milho e desoxinivalenol em trigo.
Produtos de origem animal, como carne, ovos e leite, podem ser uma fonte indireta de contaminação por micotoxinas. Sendo o leite um dos principais componentes da alimentação infantil, é merecedor de maior atenção no controle de micotoxinas, principalmente, aflatoxinas.
Considerando os efeitos crônicos que as micotoxinas podem causar, a somatória das possíveis fontes de micotoxinas na dieta humana pode representar um grave risco à saúde humana.
A literatura sugere que o melhor método para controlar a contaminação de micotoxinas em alimentos é prevenir o crescimento de fungos através da adoção de boas práticas de produção de alimentos.
REFERENCIAS BIBLIOGRÁFICAS
Almeida, A.P.; Alaburda, J.; Shundo, L.; Ruvieri, V.; Navas, S. A. Lamardo, L.C.A.; Sabino, M. Ochratoxin a in Brazilian instant coffee. Braz. J. Microbiol. v.38, p.300-303, 2007.
Amaral, K.A.S.; Nascimento, G.B.; Sekiyama, B.L.; Janeiro, V.; Machinski Jr., M. Aflatoxinas em produtos à base de milho comercializados no Brasil e riscos para a saúde humana. Ciênc. Tecnol. Aliment. v.26, n.2, p.336-342, 2006.
Bhatnagar, D.; Yu, J.; Ehrlich, K.C. Toxins of filamentous fungi. Chem Immunol. v.81, p.167-206, 2002.
Bennett, J. W.; Klich, M. Mycotoxins. Clin. Microbiol. Rev. v.16, n.3, p. 497–516, 2003.
Brasil. Resolução RDC no 274, Agência Nacional de Vigilância Sanitária, Diário Oficial da União, 16/10/2002.
Brasil. Resolução no 34/76, Ministério da Saúde, Diário Oficial da União, 19/01/1977.
Caldas, E.D.; Silva, A.C.S. Mycotoxins in Corn-Based Food Products consumed in Brazil: An Exposure Assessment for Fumonisins. J. Agric. Food Chem. v.55, p.7974–7980, 2007.
Caldas, E.D.; Silva, S.C.; Oliveira, J.N. Aflatoxinas e ocratoxina A em alimentos e riscos para a saúde humana. Rev. Saúde Pública. v.36, n.3, p.319-323, 2002.
Caldas, G.M.M.; Oliveira, R.C.; Tessmann, D.J.; Junior, M.M. Ocorrência de patulina em uva fina (Vitis vinifera L. cv. "Rubi") com sinais de podridão ácida. Ciênc. Rural. v.38, n.1, p14-18, 2008.
Calori-Domingues, M.A.; Almeida, R.R; Tomiwaka, M.M.; Gallo, C.R.; Gloria, E.M.; Dias, C.T.S. Ocorrência de desoxinivalenol em trigo nacional e importado utilizado no Brasil. Ciênc. Tecnol. Aliment. v.27, n.1, p.181-185, 2007.
Camargos, S.M.; Soares, L.M.V.; Sawazaki, E.; Bolonhezi, D.; Castro, J.L.; Bortolleto, N. Fumonisins in corn cultivars in the State of São Paulo. Braz. J. Microbiol. v.31, p. 225- 229, 2000.
Diniz, S.P.S.S. Micotoxinas. Livraria e Editora Rural. 181p. 2002.
Dors, G.C.; Pinto, L.A.A.; Badiale-Furlong E. Migration of mycotoxins into rice starchy endosperm during the parboiling process. LWT – Food Sci. Technol. v.42, p.433- 437, 2009.
Eizendeher, L.B.; Freitas, R.J.S.; Cançado, R.A. Incidência de aflatoxinas B1, B2, G1 e G2 em doces de amendoim e amendoim in natura comercializados no Estado do Paraná. Hig. Aliment. v.19, n.129, p.101-104, 2005.
Fonseca, H. Sampling plan for the analysis of aflatoxin in peanuts and corn: an update. Braz. J. Microbiol. v.33, p.97-105, 2002.
Freire, F.C.O.; Kozakiewicz, Z.; Paterson, R.R.M. Mycoflora and mycotoxins of Brazilian cashew kernels. Mycopathol. v.145, p.95-103, 1999.
Garda, J.; Macedo, R.M.; Badiale-Furlong, E. Determinação de tricotecenos em cerveja e avaliação de incidência no produto comercializado no Rio Grande do Sul. Ciênc. Tecnol. Aliment. v.24, n.4, p. 657- 663, 2004.
Gonçalez, E.; Felicio, J.D.; Pinto, M.M.; Rossi, M.H.; Nogueira, J.H.C., Manginelli, S. Ocorrência de aflatoxina M1 em leite comercializado em alguns municípios do estado de São Paulo. Arq. Inst. Biol. v.72, n.4, p.435-438, 2005.
Gonçalez, E.; Nogueira, J.H.C.; Fonseca, H.; Felicio, J.D.; Pino, F.A.; Corrêa, B. Mycobiota and mycotoxins in Brazilian peanut kernels from sowing to harvest. Int. J. Food Microbiol. v.123, p.184-190, 2008.
Hussein, S.H., Brasell, J.M,. Toxicity, metabolism, and impact of mycotoxins on humans and animals. Toxicology, v.167, n.2, p.101-134, 2001.
Kawashima, L.M.; Vieira, A.P.; Valente Soares, L.M. Fumonisin B1 and ochratoxin A in beers made in Brazil. Ciênc. Tecnol. Aliment. v.27, n.2, p.317-323, 2007.
Kawashima, L.M.; Soares, L.M.V.; Massaguer, P.R. The development of an analytical method for two mycotoxins, patulin and verruculogen, and survey of their presence in commercial tomato pulp. Braz. J. Microbiol. v.33, p. 269-273, 2002.
Kawashima, L.M.; Valente Soares, L.M. Incidência de fumonsina B1, aflatoxinas B1, B2, G1 e G2, ocratoxina A e zearalenona em produtos de milho. Ciênc. Tecnol. Aliment. v.26, n.2, p.516-521, 2006.
Iamanaka, B. T.; Menezes, H. C.; Vicente, E.; Leite, R.S.F.; Taniwaki, M.H. Aflatoxigenic fungi and aflatoxins occurrence in sultanas and dried figs commercialized in Brazil. Food Control v.18 p.454–457, 2007.
Lamardo, L.C.A.; Navas, S.A.; Sabino, M. Desoxinivalenol (DON) em trigo e farinha de trigo comercializados na cidade e São Paulo. Rev. Inst. Adolfo Lutz. v.65, n.1, p.32-35, 2006.
Leoni, L.A.B.; Furlani, R.P.Z.; Valente Soares, L.M.; Oliveira, P.L.C. Ochratoxin A in Brazilian green coffee. Ciênc. Tecnol. Aliment. v.21, n.1, p.105-107, 2001.
Mallmann, C.A.; Kowalski, C.H.; Almeida, C.A.A. Prevalência de desoxinivalenol em alimentos consumidos no Brasil. In: XII Congresso Brasileiro de Toxicologia. Anais... Porto Alegre, 2001.
Mallmann, C.A.; Santurio, J.M.; Almeida, C.A.A.; Dilkin, P. Fumonisin B1 levels in cereals and feeds from southern Brazil. Arq. Inst. Biol. v.68, n.1, p. 41-45, 2001b.
Malmann, C.A.; Dilkin, M.; Mürmann, L.; Dilkin, P.; Almeida, C.A.A. Avaliação da contaminação por desoxinivalenol em trigo utilizado na alimentação humana. In: I Congresso Brasileiro de Farmácia. Anais...São Paulo, 2003a.
Malmann, C.A.; Kowalski, C.H.; Almeida, C.A.A.; Dilkin, P.; Mürmann, L. Dilkin, M. Carvalho, R.R. Aflatoxinas em nozes e frutas secas comercializadas no Brasil. In: XIII Encontro Nacional de Analistas de Alimentos. Anais... Rio de Janeiro, 2003b.
Machinski, M.Jr.; Valente Soares, L. M.; Sawazaki, E.; Bolonhezi, D.; Castro, J.L. Bortolleto, N. Aflatoxins, ochratoxin A and zearalenone in Brazilian corn cultivars. J. Scien. Food Agricult. v.81, p.1001-1007, 2001.
Milanez, T.V.; Valente-Soares L.M.; Baptista, G.G. Occurrence of trichothecene mycotoxins in Brazilian corn-based food products. Food Control.v.17, p.293–298, 2006.
Molin, R.; Valentini, M.L. Simpósio sobre micotoxinas em grãos. Fundação Cargil. 208p. 1999.
Mürmann, L.; Kowalski, C.H.; Araujo, D.F.D.; Dilkin, M.; Dilkin, P.; Malmann, A.C. Avaliação dos índices de aflatoxinas em soja. In: V Simpósio Latino Americano de Ciência dos Alimentos. Anais... Campinas, 2003.
Murphy, P.A.; Hendrich, S.; Landgren, C.; Bryant, C.M. Food Mycotoxins: An Update. J. Food Scien. v.71, n.5, p.51-65, 2006.
Nunes, I.L.; Magagnin, G.; Bertolim, T.E.; Furlong, E.B. Arroz comercializado na região sul do Brasil: aspectos micotoxicológicos e microscópicos. Ciênc. Tecnol. Aliment. v.23, n.2, p.190-164, 2003.
Oliveira, A.Q.; Soares, L.M.V.; Sawazaki, E. Survey of deoxynivalenol, diacetoxyscirpenol and T2 toxin in popcorn hybrids panted in the state of São Paulo and in popcorn commercialized in the city of Campinas, SP. Ciênc. Tecnol. Aliment. v.21, n.3, p.330-333, 2001.
Oliveira, C.A.F.; Ferraz, J.C.O. Occurrence of aflatoxina M1 in pasteurized, UHT milk and milk powder from goat origin. Food Control. v.18, p.375–378, 2007.
Oliveira, C.A.F.; Kobashigawa, E.; Reis, T.A.; Mestieri, L. Albuquerque, R.; Corrêa, B. Aflatoxin B1 residues in eggs of laying hens fed a diet containing different levels of the mycotoxin. Food Add. Contamin. v.17, n.6, p.459-462, 2000.
Ono, E.Y.S.; Mendes, A.M.; Meirelles P.G.; Hirooka, E.Y.; Ono, M.A. Micotoxinas em alimentos: progressos na imunodetecção. Biotec. Cien. Desen. v.32, p.69-80, 2004.
Pádua, R.A.F.; Machinski Júnior, M. Aspectos toxicológicos e ocorrência de patulina em suco de maçã. Semina Cienc. Agrar. v. 26, n. 4, p. 535-542, 2005.
Peraica, M.; Radic, B.; Lucic, A.; Pavlovic, M. Efectos tóxicos de las micotoxinas en el ser humano. Bol. OMS. n.2, 2000.
Pereira, M.L.G.; Carvalho, E.P.; Prado, G. Crescimento e produção de aflatoxinas por Aspergillus flavus e Aspergillus parasiticus. B. Ceppa. v.20, n.1, p.141-156, 2002.
Pinho, B.H.; Furlong, E.B. The occurrence of molds, yeasts and mycotoxins in pre-cooked pizza dough sold in southern Rio Grande do Sul. Braz. J. Microb. v.31, p. 99-102, 2000.
Pitt, J.I. Toxigenic fungi and mycotoxins. British Med. Bul. v.56, n.1, p. 184-192, 2000.
Prado, G.; Oliveira, M.S.; Abrantes, F.M.; Santos, L.G.; Soares, C.R.; Veloso, T. Ocorrência de aflatoxina M1 em leite consumido na cidade de Belo Horizonte – Minas Gerais / Brasil – agosto/98 a abril/99. Ciênc. Tecnol. Aliment. v.19, n.3, p.420- 423, 1999.
Prado, G.; Oliveira, M.S.; Abrantes, F.M.; Santos, L.G.S.; Veloso, T.; Barroso, R.E.S. Incidência de ocratoxina A em café torrado e moído e em café solúvel consumido na cidade de Belo Horizonte, MG. Ciênc. Tecnol. Aliment. vol. 20, n.2, p.192-196, 2000a.
Prado, G.; Oliveira, M.S.; Carvalho, E.P.; Veloso, T.; Sousa, L.A.F.; Cardoso, A.C.F. Aflatoxina M1 em queijo prato e parmesão determinada por coluna de imunoafinidade e cromatografia líquida. Rev. Inst. Adolfo Lutz. v.60, n.2, p.147-151, 2001.
Prado, G.; Oliveira, M.S.; Cunha, M.R.; Gomides, M.F.; Abrantes, F.M.; Santos, L.G.; Veloso, T.; Barroso, R.E.S. Ocorrência de patulina em suco de maçã por cromatografia líquida de alta eficiência. Rev. Inst. Adolfo Lutz. v.59 n.1/2, p.21-25, 2000b.
Prado, G.; Oliveira, M.S.; Pereira, M.L.; Abrantes, F.M.; Santos, L.G.; Veloso, T. Aflatoxin M1 in samples of "Minas" cheese commercialized in the city of Belo Horizonte – Minas Gerais/ Brazil. Ciênc. Tecnol. Aliment. v.20, n.3, p. 398-400, 2000c.
Richard, J. L. Some major mycotoxins and their mycotoxicoses - an overview. Int. J. Food Microbiol. v.119, p.3–10, 2007.
Rodríguez-Amaya, D.B.; Sabino, M. Mycotoxin research in Brazil: the last decade in review. Braz. J. Microbiol. v.33, p.1-11, 2002.
Rosmaninho, J.F.; Oliveira, C.A.F.; Bittencourt, A.B.F. Efeitos das micotoxicoses crônicas na produção avícola. Arq. Inst. Biol. v.68, n.2, p. 107-114, 2001
Santin, E.; Maiorka, A.; Zanella, I.; Magon, L. Micotoxinas do Fusarium spp na avicultura comercial. Ciênc. Rural. v.31, n.1, p.185- 190, 2000.
Santurio, JM. Micotoxinas e Micotoxicoses na Avicultura. Rev. Bras. Cienc. Avic. v.2, n.1, p.01-12, 2000.
Sassahara, M.; Netto, D.P.; Yanaka, E.K. Aflatoxin occurrence in foodstuff supplied to dairy cattle and aflatoxina M1 in raw milk in the North of Paraná state. Food Chem. Toxicol. v.43 p. 981-984, 2005.
Scussel, V.M. Comparison of methods by TLC and HPTLC for determination of aflatoxin M1 in milk and B1 in eggs. Cienc. Tecnol. Aliment. v.23, p.26-52, 2003.
Sekiyama, B.L.; Ribeiro, A.B.; Machinski, P.A.; Junior, M.M. Aflatoxins, ochratoxin A and zearalenone in maize-based food products. Braz. J. Microbiol. v.36, p.289- 294, 2005.
Shephard, G.S. Impact of mycotoxins on human health in developing countries. Food Add. Contam. v.25, n.2, p.146–151, 2008.
Shundo, L.; Almeida, A.P.; Alaburda, J.; Ruvieri, V.; Navas, S.A.; Lamardo, L.C.A.; Sabino, M. Ochratoxin A in wines and grape juices commercialized in the city of São Paulo, Brazil. Braz. J. Microbiol. v.37, p. 533-537, 2006.
Silveira, S.M.; Maixner, A.E.; Fontana, F.Z.; Almeida, C.A.; Stefanon, E.B.; Santurio, J.M.; Malmann, C.A. Determinação de aflatoxina B1 e M1 no fígado de aves. In: III Jornada Integrada de Pesquisa, Extensão e Ensino. Anais... Santa Maria, 1996.
Simionato, E.M.R.S.; Astray, R.M.; Sylos, C.M. Ocorrência de ocratoxina A e aflatoxinas em arroz. Rev. Inst. Adolfo Lutz. v.62, n.2, p.123 – 130, 2003.
Stamford, T.L.M.; Vilar, E.A.; Bastos, S.T.G.; Silva, C.G.M. Pesquisa micotoxicológica de produtos avícolas "in natura" e processados. B. Ceppa, v.23, n.1, p.135-160, 2005.
Vilar, E.A.; Oliveira, M.C.M.; Stamford, T.L.M. Pesquisa micotoxicológica em fígado de aves produzidas e comercializadas em Pernambuco. B. Ceppa. v.20, n.2, p. 335-346, 2002.
***O Trabalho foi originalmente publicado pela Revista Brasileira de Produtos Agroindustriais, Campina Grande, v.12, n.1, p.89-99, 2010 ISSN 1517-8595